
8月31日,FDA针对洁定(Getinge)公司的Cardiosave混合主动脉内球囊泵(IABP)和Cardiosave 救援主动脉球囊泵IABP,一天内连发四条一级召回召回!要知道,该产品此前已经被召回5次了!

图片来源:FDA官网
该设备的内部温度超过176华氏度时,它们可能会过热。发生这种情况时,设备将生成“系统过温”警报,将设备置于待机模式。然后,泵停止提供治疗。
在2021年1月1日至2023年6月2日期间,洁定报告了213起投诉,包括4人受伤和1人死亡。
该设备在自动填充故障警报可能会使设备处于待机模式,导致治疗中断。当IABP治疗开始时,IABP会自动用氦气填充气球导管回路。每两小时或大气压力变化期间,就会发生IABP自动填充过程。
如果自动填充过程的任何步骤失败或未完成,设备将生成“自动填充失败”警报消息,IABP泵将停止提供治疗。如果警报持续,患者可能会经历长时间的治疗中断,这将需要医疗保健提供者获得不同的控制台才能继续治疗。
如果另一个IABP控制台无法使用,医疗保健提供者可能会启动提供血流动力学支持的替代手段(血管抑制剂、各向异性或替代疗法),作为临时措施。
在2021年1月1日至2023年6月2日期间,洁定报告了298起与该设备问题相关的投诉,包括两人死亡和多达3人受伤。
该设备由于气体增益或气体损失发生警报时,泵可能会意外停止。警报将中断治疗,并需要用户干预来纠正和重新启动。如果警报持续,则必须将设备切换到备用IABP以继续治疗。如果没有备用IABP,医疗保健专业人员必须寻求提供血流动力学支持的替代方法。这可能包括临时使用血管抑制剂、各异位肌或其他替代疗法。
警报可能是由患者运动(如咳嗽、一般运动和吞咽);回路中的血液;或与管道/导管的连接松动、扭结或磨损引起的。此外,发烧或心跳加速的患者可能会经历更高的气体流失率,这可能会导致警报。
在2021年1月1日至2023年6月2日期间,洁定报告了198起与该设备问题相关的投诉,包括三名受伤和两名患者死亡的设备。
该设备与IABP控制台与购物车(混合模式)的对接不正确相关的意外关闭。如果Cardiosave IABP没有正确地停靠在购物车中,它将无法获得交流电源,并将意外地在电池供电(救援模式)下运行,并在电池耗尽时关闭。此外,如果Cardiosave IABP没有正确停靠在手推车上(混合模式),Cardiosave将无法为插入的电池充电,并可能影响安全运输患者的能力。
在2021年1月1日至2023年6月2日期间,Getinge/Maquet/Datascope报告了533起投诉,包括1人死亡。
FDA一次性发布了四条关于洁定Cardiosave混合主动脉内球囊泵(IABP)和Cardiosave 救援主动脉球囊泵 IABP的一级召回,主要可能源于这些情况都出现在同一批次的设备中:2012年3月6日至2023年5月19日,在美国分发的设备批次中,共4586台。
据统计,在总共发行了4586台的这批次中,已经收到了1242次投诉,这意味着近27%的产品出现了问题。这一比例相当高,表明产品可能存在严重的质量问题。更令人震惊的是:已有10人受伤,6人死亡。
这些数据足以证明该产品存在严重的安全隐患,结合之前的五次召回来看,这款产品可能需要的不是一次又一次的召回,而是技术的升级与安全性的提升。
洁定(Getinge)这个产品之前已经被召回五次!
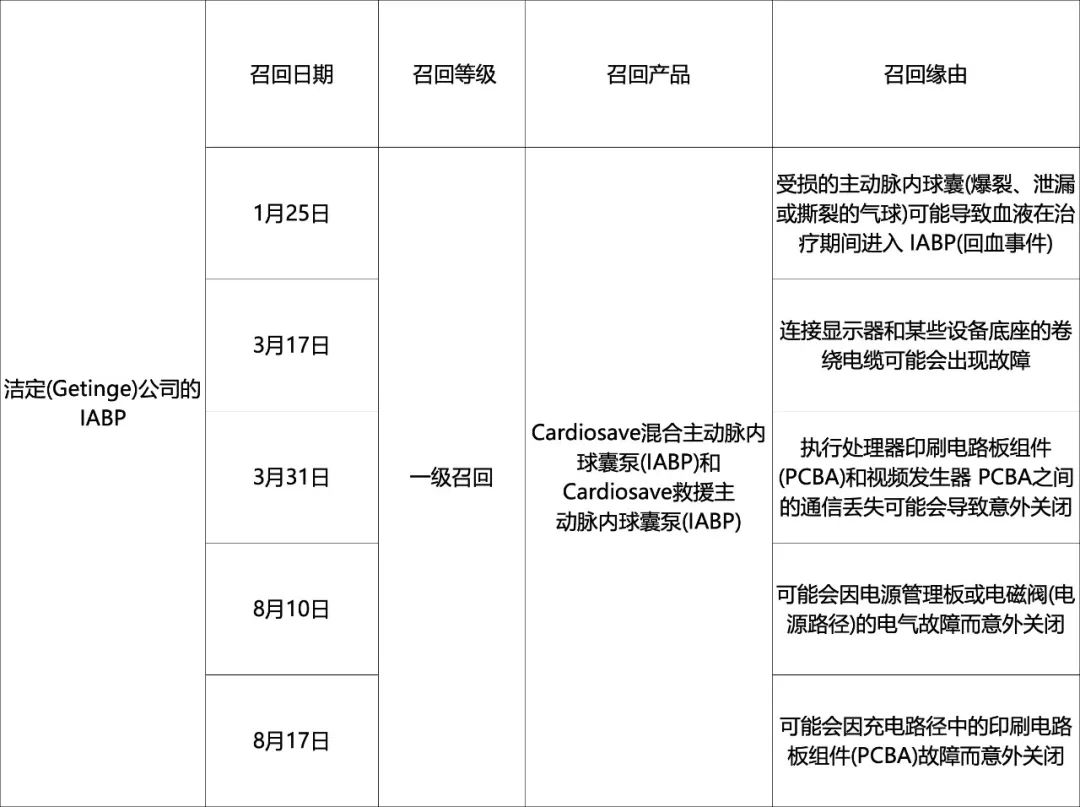 图表来源:医疗器械创新网整理
Cardiosave混合主动脉内球囊泵(IABP)和Cardiosave 救援主动脉球囊泵 IABP是用于充气和放气主动脉内球囊的机电系统。这些系统通过反脉动为左心室提供临时支撑。一旦球囊位于主动脉中,泵将与心电图或动脉压力波形同步工作,使球囊在心脏周期的适当时间充气和放气。
图表来源:医疗器械创新网整理
Cardiosave混合主动脉内球囊泵(IABP)和Cardiosave 救援主动脉球囊泵 IABP是用于充气和放气主动脉内球囊的机电系统。这些系统通过反脉动为左心室提供临时支撑。一旦球囊位于主动脉中,泵将与心电图或动脉压力波形同步工作,使球囊在心脏周期的适当时间充气和放气。
Cardiosave主动脉内球囊泵适用于急性冠脉综合征、心脏和非心脏手术,或成人心力衰竭并发症。它们用于医疗保健设施。
此次FDA一级召回主要是因为,主动脉内球囊受损(气球爆裂、泄漏或撕裂)可能导致血液在治疗期间进入IABP(回血事件)。泵中的血液可能导致以下问题:
-
如果血液与电气部件接触,泵会意外关闭。泵关闭可能导致血流不稳定(血流不稳定性)、器官损伤和/或死亡,特别是对于重症患者和最有可能使用这些设备接受治疗的人来说。
-
如果继续治疗,患者可能会将氦释放到血液中。血液中的氦气气泡(气栓塞)会损害器官(包括大脑)。
-
-
如果不采取适当的遏制预防措施,用户和/或随后的维护或服务人员可能会面临意外的生物危害。
-
如果在与新患者一起使用之前没有对受影响的IABP进行评估,则该新患者可能会接触到交叉污染的血液,这也使他们暴露在潜在的终身细菌和病毒性疾病中,如乙型肝炎、丙型肝炎和艾滋病毒。
洁定这次事件报告了134起关于这个问题的投诉,包括12起设备关机和5起不良事件(4起严重受伤和1起死亡)。
此次FDA一级召回主要是因为,连接显示器和某些设备底座的卷绕电缆可能会出现故障,导致意外关机。这种关机将不会发生警告或警报来提醒用户。一旦发生错误,需要更换盘绕的电线才能让设备再次工作。这个问题可能发生在2017年7月24日之前分发的单位中。
意外的泵关闭和治疗的任何中断都可能导致血流不稳定(血流不稳定性)、器官损伤和/或死亡,特别是对于重症患者和最有可能使用这些设备接受治疗的人。
从2019年6月到2022年8月, 洁定报告了44起关于卷绕线损坏导致意外关机的投诉。没有与这个问题有关的伤亡报告。
此次FDA一级召回主要是因为,执行处理器印刷电路板组件(PCBA)和视频发生器PCBA之间的通信丢失可能会导致意外关闭。这种关机将不会发生警告或警报来提醒用户。一旦发生错误,需要更换一个或两个PCBA才能使设备再次工作。
泵的意外关闭和治疗的任何中断都可能导致血流不稳定(血流不稳定性)、器官损伤和/或死亡,特别是对于重症患者和最有可能使用这些设备接受治疗的人。
洁定报告了42起关于PCBA通信故障导致意外关机的投诉。没有与这个问题相关的任何伤亡报告。
此次FDA一级召回主要是因为,它们可能会因电源管理板或电磁阀(电源路径)的电气故障而意外关闭。
使用受影响的泵可能会导致严重的不良健康事件,包括血压不稳定、受伤(例如:血液供应不足或重要器官损伤)和死亡。
此次FDA一级召回主要是因为,它们可能会因充电路径中的印刷电路板组件(PCBA)故障而意外关闭。如果发生这种情况,由于电源管理板充电路径电路中的电涌损坏,设备可能会失去为一个或两个电池托架/插槽中的电池充电的能力。
洁定报告了252起投诉。没有关于受伤或死亡的报告。
2020年,全球主动脉内球囊反搏泵(IABP)市场规模达到了3.44亿美元,预计2027年将达到4.30亿美元,年复合增长率(CAGR)为3.37%。
北美市场主导全球主动脉内球囊反搏泵(IABP)市场,因为其较高的可支配收入、先进完善的医疗基础设施和不断增长的心血管手术案例。主动脉内球囊反搏泵(IABP)在欧洲和北美的使用率较高,相比之下,在亚太地区、中东和非洲、南美洲和中美洲地区有很大的增长潜力。未来几年,中国、印度、东南亚、巴西和墨西哥等地区产品需求的增长将促进市场增长。
主动脉内球囊反搏泵(IABP)可分为常规IABP和光纤IABP,其中常规IABP占比最高,2020年收入占比达71%。
可分为医院和心脏监护中心等,其中医院是主动脉内球囊反搏泵(IABP)是主要的应用领域,2020年占比达到80%。
目前全球主要厂商包括洁定(Getinge Group)、泰利福(Teleflex)和泉工医科工業株式会社(Senko Medical Instrument Mfg. Co., Ltd (MERA)),2020年洁定份额占比超过80%,预计未来几年行业竞争将保持稳定。
目前国内主动脉内球囊反搏泵(IABP)全部进口于国外三个品牌,目前市面上尚无自主品牌的IABP产品,国内无产品出口,全部依赖于进口。
期望在未来,国内制造商能够加强研发力度,推出自主品牌的IABP产品,打破目前的进口依赖局面,进一步促进国内医疗设备行业的健康和可持续发展
|信息来源:FDA官网,医疗器械创新网编译、数据来源于恒州诚思YH