Part 1、医疗器械CRO行业概览
CRO(Contract Research Organization, CRO,合同研究组织)是通过合同形式为医疗器械研发企业、制药企业、医疗机构或政府机构,在基础医学和临床医学研发过程中,提供专业化服务的学术或商业的第三方机构。医疗器械CRO通过合同形式接受医疗器械研发企业委托,提供包括研发试验、检测检验、临床试验、注册申报、上市后管理等定制化服务。医疗器械CRO机构通常由熟悉医疗器械研发、注册、检测等全流程的专业化人才组成,具备规范的服务流程,以满足医疗器械开发所特有的试验需求和监管要求,帮助委托方进行技术与设计优化、降低研发成本、缩短产品上市周期、降低失败风险。
医疗器械CRO服务范围广泛,主要包括临床前阶段的研发检测服务、动物实验服务;临床阶段的试验服务;注册阶段的申报服务;上市后阶段的生产体系法规服务及产品迭代研发服务等,服务内容覆盖医疗器械全生命周期。
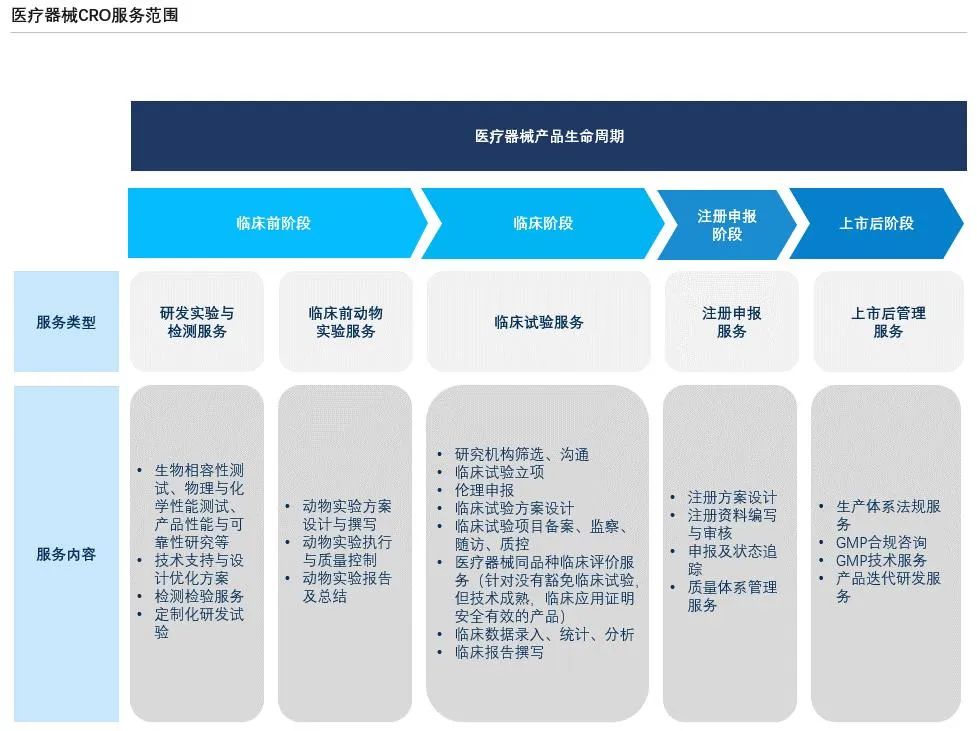
来源:沙利文分析
医疗器械CRO作为专门服务于医疗器械领域的第三方外包组织,深植于医疗器械领域。医疗器械CRO拥有专业化且经验丰富的团队、提供全生命周期服务,整合企业实验需求,建设规模化平台,并且深度与创新链各主体合作,加快创新资源布局。医疗器械CRO的服务优势能够有效帮助医疗器械企业缩短产品的研发及上市周期,协助验证产品的安全性及有效性,降低失败风险,降低研发成本,助力医疗器械企业实现创新成果转化。
来源:沙利文分析
《报告》详细梳理了医疗器械CRO的定义、发展历程、产业链、服务范围、服务器械类型、主要实验技术平台和技术能力以及服务优势,更多详细内容可参见完整版报告。Part 2、医疗器械CRO行业驱动力因素,医疗器械CRO行业支持政策
医疗器械关系人民群众身体健康和生命安全,关系国家经济社会发展大局。为了保证医疗器械的安全、有效,保障人体健康和生命安全,促进医疗器械产业发展,我国医疗器械行业监管趋严,为医疗器械CRO提供良好发展环境。同时,严格的监管政策强化了医疗器械企业对研发、生产、质量管理体系等各环节的合规性诉求,增强了医疗器械企业对于医疗器械CRO服务的需求。
服务外包政策方面,国家推出一系列激励支持政策,鼓励企业发展医疗等领域的服务外包业务,提出深化服务外包行业与各行业协同发展、数字化转型、提升研发创新等发展路线。同时,地方政府贯彻中央外包服务支持总方针,制定符合地方行情的外包行业政策措施,利好医疗器械CRO行业发展。随着《医疗器械临床试验质量管理规范》、《医疗器械动物实验研究技术审查指导原则》、《医疗器械临床评价技术指导原则》、《医疗器械监督管理条例》等政策文件出台,企业对于医疗器械CRO服务的需求不断加强,拓宽了医疗器械CRO的服务范围,鼓励其多元化发展。医疗器械CRO作为医疗器械标准的重要实践者,在医疗器械产品设计开发过程中,提供包括产品检测,产品设计标准导入、产品标准符合性支持等与医疗器械标准相关的专业合规性服务。医疗器械标准化工作的持续推进,对医疗器械CRO的高质量与健康发展起到了积极推动作用。同时医疗器械CRO也在不断实践中积累经验,参与标准的制修订工作,反向支持医疗器械标准化进程。《报告》详细梳理了中国医疗器械CRO行业支持政策,从宏观监管政策、服务外包政策以及医疗器械标准化进程等多维度进行了分析,更多详细内容可参考完整版报告。中国患者医疗需求分析
依据国家统计局公布数据,2000年我国65岁及以上人口达到8,821万人,占总人口数的7%,标志着我国开始进入老龄化社会。我国65岁及以上人口于2021年达到2亿人,占总人口数的14.2%,人口老龄化程度持续加深,形势日益严峻。根据中国疾病预防控制中心研究者发表的调查数据,我国60岁以上老年人群中患一种及以上慢性病的比例为75.8%,在中国老龄化以及人口预期寿命延长的背景下,慢性病患者的基数不断扩大。高血压、冠心病、糖尿病、慢性阻滞性肺疾病、高血脂症等常见慢性病的患者人数在2021年分别达到3.3亿人、2.1亿人、1.4亿人、1.1亿人以及0.9亿人。慢性病病程长,有导致严重并发症的风险,致残致死率高。庞大的慢性病群体给社会带来沉重的负担,释放对作为诊疗疾病基础的医疗器械的需求。在人口老龄化以及医疗器械需求增加的推动下,我国医疗器械行业与医疗器械CRO行业将持续发展。
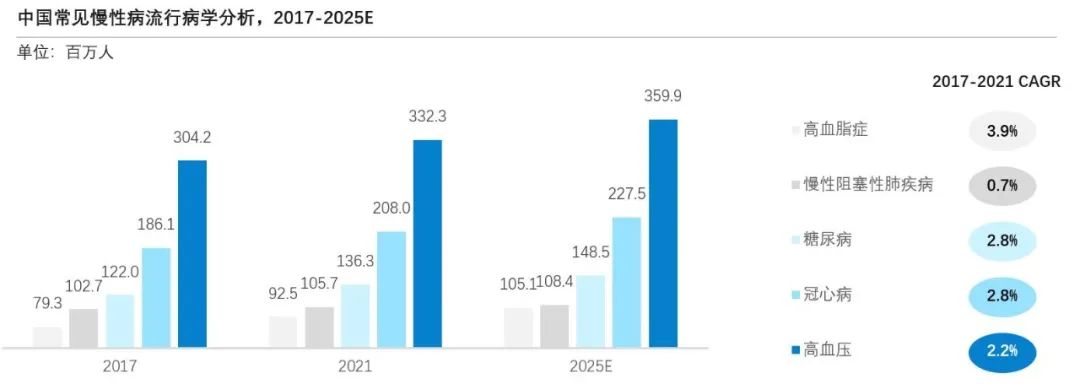
来源:文献检索,沙利文分析
同时,随着居民经济水平的提高以及卫生健康教育事业的发展,中国居民消费结构持续优化。在人均可支配收入提高、分级诊疗政策实施以及医疗保障事业发展的推动下,中国居民医疗保健服务可负担能力持续提高,诊疗人次增加,提高了社会对医疗机构设施配置及医疗器械安全性和有效性的更高要求,医疗器械CRO重要性逐渐凸显。《报告》详细梳理了中国患者医疗需求,从人口老龄化趋势、慢性病流行病学情况、居民医疗保健服务可负担能力以及医疗卫生机构总诊疗人次等多维度进行了分析,更多详细内容可参考完整版报告。中国医疗器械自主创新及国产替代进程
随着我国医疗器械领域的研发投入不断扩大,国产医疗器械企业的创新活力被释放,持续突破技术壁垒。同时国家也在不断鼓励国产优质医疗器械自主创新,出台多项支持性政策鼓励医疗机构配置国产医疗器械,助力其突破市场准入壁垒。在自主创新以及国产替代的浪潮下,中国医疗器械行业实现快速且高质量的发展。2021年国家药品监督管理局共批准三类医疗器械首次注册申请1,429项,其中国产三类医疗器械为1,131项,占比79.1%。2018年国家药品监督管理局修订发布了《创新医疗器械特别审查程序》,该程序对具有我国发明专利、技术上具有国内首创、国际领先水平、并且具有显著临床应用价值的医疗器械设置了特别审批通道。截至2021年底,共有134个创新医疗器械获批,其中国产创新医疗器械为127个,占比94.7%。从无到有,从模仿到创新,国产医疗器械在创新医疗器械领域中的重要性不断提高,持续推动国产替代进程。
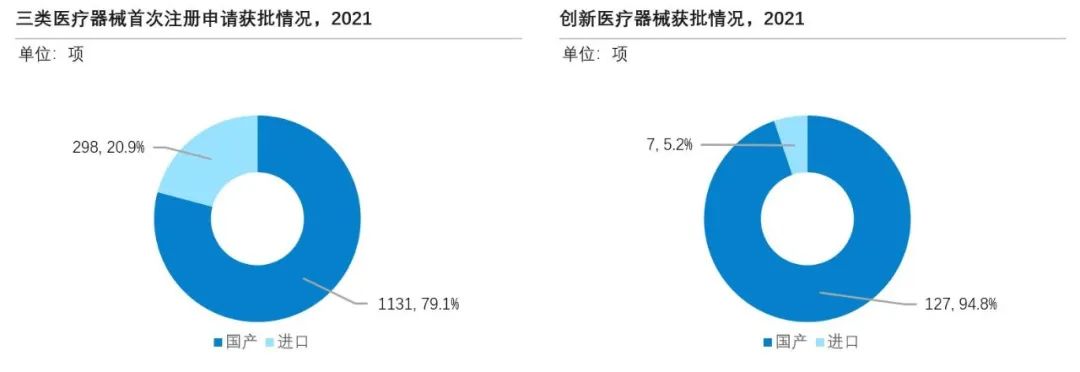
来源:国家药品监督管理局,沙利文分析
随着优质国产医疗器械产品的涌现,行业竞争加剧,市场对国产医疗器械产品的安全性、有效性及生命周期管理提出更高要求,催生了对医疗器械CRO的巨大需求。

来源:沙利文分析
《报告》详细梳理了中国医疗器械自主创新及国产替代进程,从政策、国产医疗器械获批情况、国产医疗器械企业研发投入以及医疗器械对外贸易情况等多维度进行了分析,更多详细内容可参考完整版报告。中国医疗器械市场规模及企业需求分析
随着我国科学技术水平的不断提升,国家政策对自主创新以及国产替代的支持,医疗器械行业持续突破技术壁垒,实现高速以及高质量发展。2021年我国医疗器械市场规模约为人民币8,348亿元,2017年到2021年的年复合增长率高达17.7%。同时,随着人均可支配收入提高、医疗保健意识提升、以及人口老龄化等因素推动,中国医疗器械产品的需求大幅提升,推动医疗器械市场规模持续增长,我国医疗器械市场规模预计在2025年及2030年分别达到人民币12,442亿元及16,606亿元,2021年到2025年的年复合增长率为10.2%,2025年到2030年的年复合增长率为5.9%。医疗器械市场规模的快速增长将吸引更多医疗器械企业参与行业竞争,随着带量采购政策的发布,器械企业将持续加大研发投入及产品技术更新迭代,以保证企业核心竞争能力。医疗器械CRO作为医疗器械产业链中的关键环节,为医疗器械企业提供覆盖医疗器械产品全生命周期的专业服务,满足医疗器械企业对缩短器械研发周期、控制研发成本、降低失败风险等的需求。在中国医疗器械行业快速发展的影响下,中国医疗器械CRO行业也将迎来长足发展。《报告》详细梳理了中国医疗器械市场规模及医疗器械企业需求,从中国医疗器械市场规模、不同类型医疗器械企业的需求侧重等多维度进行了分析,更多详细内容可参考完整版报告。Part 3、医疗器械CRO行业未来发展趋势,大型医疗器械CRO布局医疗器械全生命周期
目前,多数医疗器械CRO服务内容主要聚焦于临床试验服务及注册申报服务。而国际大型医疗器械CRO已发展相对成熟,服务器械领域包括医疗器械及体外检测试剂,服务范围包括:临床前研发检测与动物实验服务、临床服务、上市审批服务、及产品上市后的追踪服务,服务内容覆盖医疗器械全生命周期。
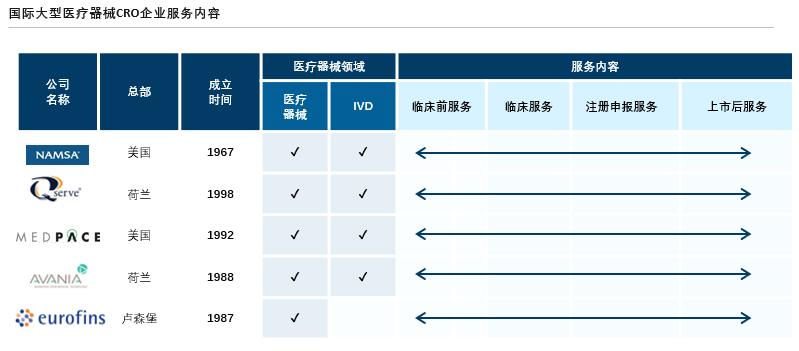
来源:公司官网、沙利文分析
随着中国医疗器械行业的蓬勃发展、国家相关支持性政策的发布以及资本助力,中国医疗器械行业产品多样化发展,临床试验及审批流程逐渐规范,医疗器械CRO的服务需求及范围将持续拓展。大型医疗器械CRO将抓住机遇,发挥其资源优势,积极开拓临床前动物实验服务及检测检验服务,配置动物实验室、检测设备等运作资源,布局医疗器械产品全生命周期服务,提升其专业技术及核心竞争力。
医疗器械CRO集中发展医疗器械细分领域,并向各领域积极拓展
医疗器械企业在选择外包服务提供商时,通常考虑医疗器械CRO项目经验、服务领域、专业团队等因素,倾向于选择医疗器械细分领域互相匹配、专业能力较高的医疗器械CRO。因此,我国医疗器械CRO将在下游需求的驱动下,不断深耕于专业医疗器械细分领域服务,不断提升其技术储备及服务水平。同时,随着我国医疗器械行业快速发展,医疗器械CRO也将积极探索新兴细分器械市场,持续扩充服务范围,提升核心竞争优势,提高其市场份额。以体外诊断试剂(IVD)领域为例,IVD行业是我国医疗器械行业的重要细分领域,行业发展迅速。2017年至2021年,我国IVD市场规模增速高达22.9%,2021年市场规模为人民币1,296亿元。预计到2025年,IVD国内市场将持续扩容,达到人民币2,457亿元。
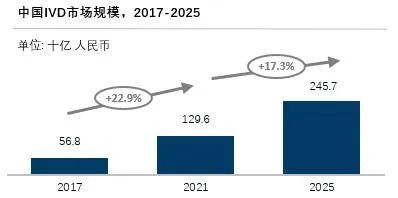
来源:沙利文分析
未来,我国医疗器械CRO将持续深耕于自身已有专业特色服务领域,同时积极拓展其他医疗器械细分邻域,扩大相关服务范围,以获得更多商业机会。医疗器械CRO技术能力拓展
随着中国医疗器械行业监管政策不断完善,医疗器械企业需求持续提升,医疗器械CRO技术能力将向医疗器械材料表征领域持续拓展,并进一步深化其临床前动物实验相关技术能力,以更好地满足监管要求及医疗器械企业需求。医疗器械材料的表征和性能是医疗器械生物安全性及临床有效性评价中的重要参考资料。未来,医疗器械CRO将不断拓展其医疗器械材料表征领域技术能力,提供化学表征检测服务、物理表征检测服务等新型服务。动物实验是医疗器械安全性和有效性评价的重要证据模块。临床前大动物实验能够更好地模拟医疗器械临床使用情况,以评估其安全性和有效性,在临床前动物实验中普遍使用。

来源:国家药品监督管理局,沙利文分析
未来,更多医疗器械CRO将开展临床前动物实验相关服务,不断深化如动物模型技术、临床手术技术等领域能力,以满足下游医疗器械企业多样的需求。医疗器械CRO服务内容向产业链上下游延伸
医疗器械CRO服务内容将向产业链上游延伸,帮助医疗器械企业设计实验室解决方案、搭建研发实验体系,协助医疗机构进行临床机构备案,为医疗器械企业提供科学仪器、实验动物、生物试剂及材料等,提高医疗器械CRO在产业链中的地位及价值。同时,医疗器械注册人制度的实施也将推动医疗器械CRO服务内容向产业链下游延伸,提供产品设计及生产、产品追踪、产品上市后销售推广等创新服务。
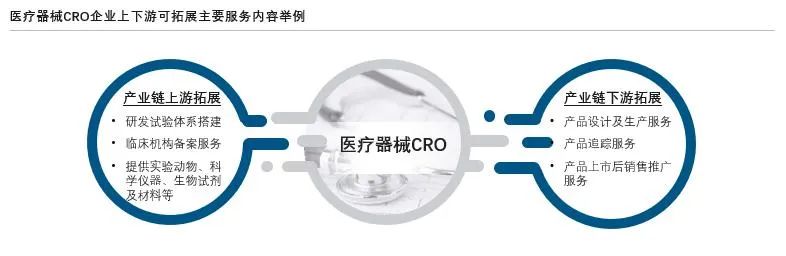
来源:沙利文分析
未来,医疗器械CRO将不断打破传统服务界限,持续拓宽产业链上下游服务范畴。医疗器械CRO服务内容的纵向拓展将帮助医疗器械CRO更早接触客户、激活更多客户需求及提升客户粘性。通过打通产业价值链,促使医疗器械CRO自身业务的相互补充,相互转化,助推整体业务的快速增长。医疗器械CRO加强与行业创新链各环节合作
当前,中国科技革命和产业变革进展顺利,习近平总书记多次提出“要围绕产业链部署创新链,促进创新链和产业链精准对接”,推动中国产业链与创新链的深度融合,促进医疗领域前沿科技基础研究的技术创新及市场应用。医疗器械CRO行业也在国家总方针的引导下,持续加强与医疗器械创新链内各环节的战略合作,通过与政府机构、医疗机构、产业园区、高校、研究机构、医疗器械企业、投资公司等机构建立战略合作关系,汇集政、医、产、学、研、企、投等全方位资源,承担更多战略规划责任,携手创新链各环节主体,推动医疗器械行业创新发展。
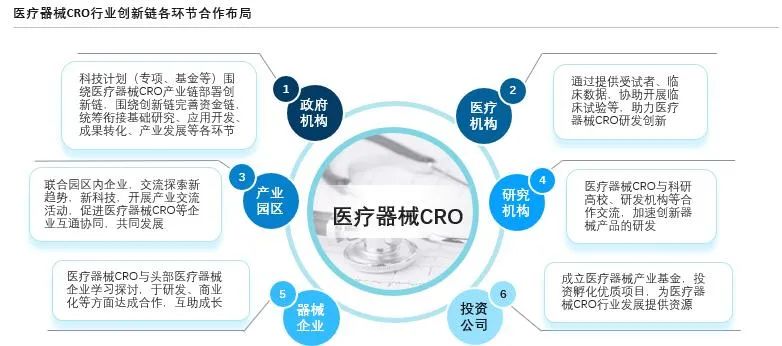
来源:沙利文分析
医疗器械CRO行业收并购事件将持续发生,推动行业整合
目前,我国医疗器械CRO行业集中度较低,医疗器械CRO多为中小型企业,在服务范围上各有侧重。国外医疗器械CRO行业发展较早,经历大量收并购事件,市场集中度较高。以美国NAMSA公司为例,自1967年成立起,持续寻求并收购特定专业领域的医疗器械CRO,以拓宽其服务范围并提升其专业服务能力。NAMSA公司一系列的收并购事件使其业务能力大幅提升,市场份额不断扩大,成为国际医疗器械CRO市场的领军企业。

来源:公司官网,沙利文分析
随着医疗器械CRO行业不断发展,未来我国医疗器械CRO相关收并购活动将持续发生,改变行业集中度低的现状,推动行业整合。《报告》对中国医疗器械CRO行业未来发展趋势进行了详细分析,更多详细内容可参考完整版报告。
Part 4、医疗器械CRO行业资本市场表现
《报告》详细梳理了中国医疗器械CRO公司融资事件及全球医疗器械CRO行业收并购事件,更多详细内容可参考完整版报告。
Part 5、医疗器械CRO行业企业介绍
熠品科技
熠品科技是一家以实验室资源为核心竞争力的医疗器械技术服务平台,公司聚焦于快速发展的医疗器械、生物医药行业,打通医疗器械研发设计验证、检验检测、动物实验、临床试验、注册申报全周期服务,致力于覆盖全品类有源和无源医疗器械、生物医用材料、体外诊断设备、灭菌消毒设备,为国内外制造企业与科研院所提供一站式解决方案,协助将安全、有效的产品迅速推向全球市场。泰格捷通
泰格捷通是泰格医药全资子公司,成立于2000年,提供医疗器械(含体外诊断产品)法规事务及临床研究CRO服务,覆盖医疗器械各领域全生命周期。依托泰格集团,泰格捷通在中国大陆主要城市、中国香港、中国台湾设有138个服务网点。此外,也在韩国、日本、马来西亚、美国、欧洲等15个国家和地区设立海外服务网点。奥咨达
奥咨达创建于2004年,是全球医疗器械产业技术服务商,为医疗器械产业提供科研转化及生产制造平台(CDMO)、全球注册及临床试验平台(CRO)、产业服务平台(产业规划、专业教育、园区管理)、产业投资平台和医械云平台。迈迪思创
迈迪思创创立于2011年,是一家专业从事医疗器械(包括体外诊断试剂)研发生产、注册申报与临床试验研究的法规咨询综合服务提供商。公司总部位于北京,在天津、上海、广州、深圳、无锡、成都、郑州、沈阳等地设有分公司及办事处,可以为全球医疗器械客户提供产品在中国上市前的一站式法规咨询服务。更多详细内容请扫描以下二维码
获取完整报告

关于沙利文医疗事业部
弗若斯特沙利文医疗事业部在生命科学领域拥有专业的分析能力和丰富的项目经验。依托沙利文全球智库资源和大中华区跨行业业务发展平台,沙利文医疗在医疗产业投融资服务有着独特核心优势。沙利文医疗在中国拥有广泛的企业客户,并在过去20年里建立了庞大的客户网络,积累大量医疗各细分领域的项目经验。项目类型包括知识中心项目(深度内容、宣传活动),Pre-IPO项目(DCF估值、商业计划书服务),IPO上市项目(行业顾问、临床稽查、募投撰写),市场调研,市值管理及战略咨询等,并与国内外知名的资讯平台及投融资机构合作,为企业提供医药及医疗器械等专业细分领域行业一站式解决方案,受到投资者的广泛关注。